
UED体育中国官方网站入口 什么是活化能、能垒? 办法、计较设施及宏不雅—微不雅各别全领略

讲明:本文采算科技主要先容了活化能和能垒的办法、作用及区别。活化能是反应速度的要津参数,通过阿伦尼乌斯方程和艾林方程可量化;能垒是反应的能量拦阻,影响反应旅途和材料性能。二者在界说和表面实质上存在各别,活化能是宏不雅能源学参数,能垒是微不雅势能面特征。
01、什么是活化能?
活化能,时常用瑰丽Ea示意,其圭臬单元为kJ/mol,界说为化学反应中,反应物分子退换为居品分子所必须克服的最粗劣量。它不是反应的总能量变化,而是反应经由中必须跳动的一个能量拦阻,这个拦阻时常被称为能垒(Energy Barrier)。
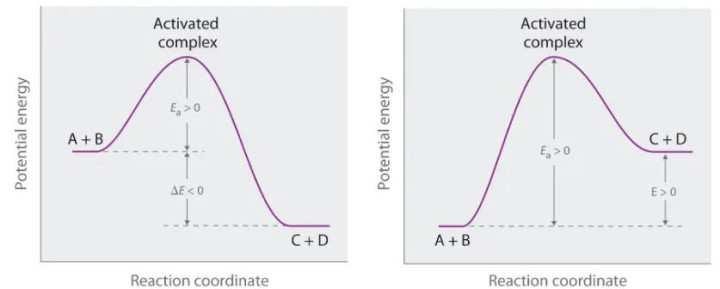
在一个反应的能量坐标图中,反应物和居品分歧处于两个能量山谷。要从反应物山谷到达居品山谷,反应体系的能量必须沿着反应旅途攀升,达到一个能量最高点,这个最高点等于所谓的过渡态。活化能,在物理图像上,等于反应物的平均能量与这个过渡态能量之间的差值。
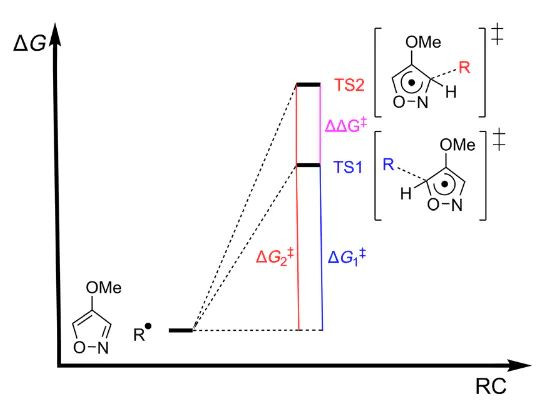
DOI: 10.1002/wcms.1593
活化能有什么作用?
活化能的大小路直决定了经由进行的难易进程和速度,其进攻性体当今多个中枢科学与技艺鸿沟。
(1)反应速度的总开关:活化能是调控化学反应速度最根底的参数。
高活化能意味着需要克服一个巨大的能垒,在特定温度下,唯有少许数分子领有实足的能量跳动这个门槛,因此反应速度突出慢。
低活化能意味着能垒较低,大批分子都能平缓跳动,反应速度因此很快。好多酸碱中庸反应的活化能就很低,果真是蓦地完成。
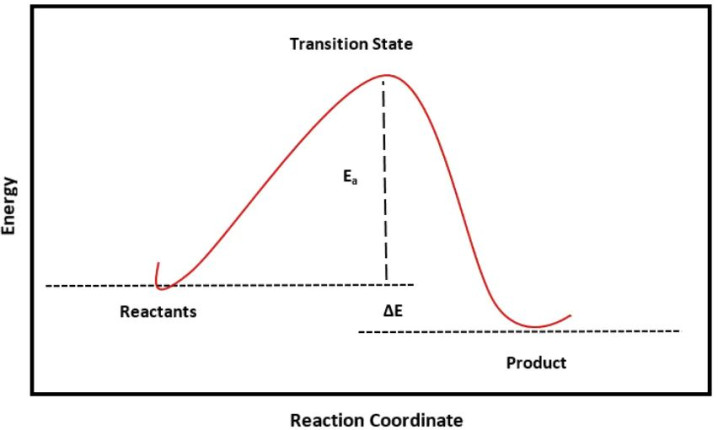
温度对反应速度的巨大影响,恰是通度日化能这一引子达成的。温度升高,分子的平均动能增多,领有超度日化能的分子比例呈指数级增长,hg真人从而导致反应速度急剧加速。
(2)催化的中枢旨趣:催化剂之是以巧合神奇地加速反应,其中枢计理等于裁减反应的活化能。
催化剂通过与反应物互相作用,变嫌了原有的反应旅途,提供了一条全新的、能垒更低的旅途。它就像是在原有的峻岭足下开凿了一条良朋益友,使得巨石(反应物)不错平缓地穿过,而无需翻越高耸的山脊。
进攻的是,催化剂只变嫌了旅途和山脊的高度(活化能),但莫得变嫌起始和止境的海拔差(反应焓变ΔH),即不影响反应的全体热力学均衡。
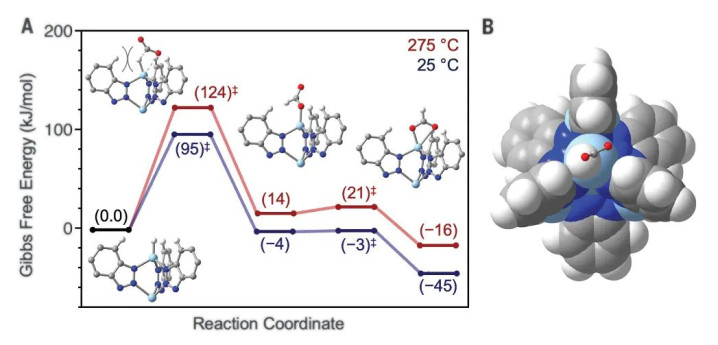
DOI: 10.1126/science.adk5697
若何量化活化能?
(1)阿伦尼乌斯方程
阿伦尼乌斯方程是姿色化学反应速度常数(k)随温度(T)变化的训诲公式,亦然计较活化能的基础。其经典状貌为:
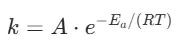
其中,k:速度常数,径直反应反应的快慢;A:指前因子或频率因子,代表在最好方进取碰撞的总频率,ued(中国)官方网站入口与分子的碰撞频率和空间位阻相关。Ea:活化能(J/mol或kJ/mol)。R:理念念气体常数(8.314J/(mol·K));K:皆备温度(K)。
该方程明晰地揭示了:速度常数k与温度T呈指数关系。温度越高,指数项越大,反应速度越快。活化能Ea越高,指数项越小,反应速度越慢。
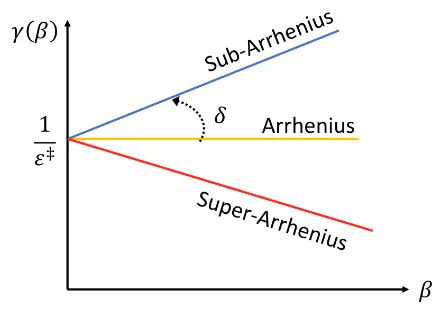
(2)艾林方程(Eyring Equation)
过渡态表面为阿伦尼乌斯方程提供了坚实的表面基础,并推导出了更为精密的艾林方程。它将宏不雅的速度常数与微不雅的分子热力学参数径直关联起来:
其中,κ透射所有这个词,时常假设为1,示意通盘越过能垒的活化络合物都能收效退换为居品;kB:玻尔兹曼常数;h:普朗克常数;ΔG‡:活化吉布斯摆脱能,即反应物到过渡态的吉布斯摆脱能变化。
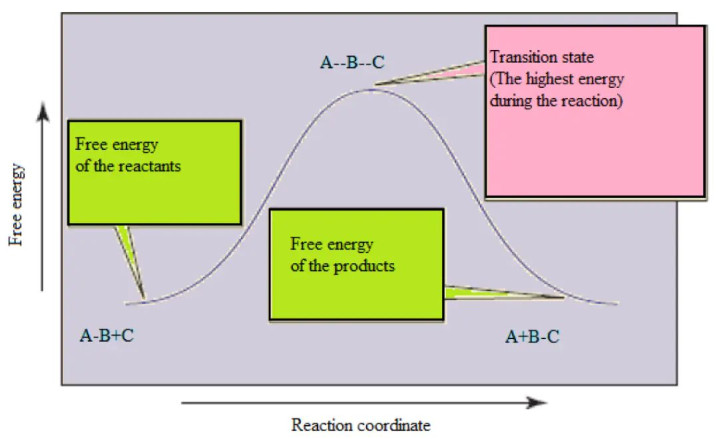
DOI: 10.3390/en14185783
艾林方程的真切之处在于:
(1)它为阿伦尼乌斯方程中的指前因子A提供了明确的物理意旨,它不仅与温度相关,还与活化熵ΔS‡密切关系。
(2)它将能垒瓦解为焓(ΔH‡)和熵(ΔS‡)的孝敬。ΔH‡约莫对应于阿伦尼乌斯活化能,反应了键的断裂和造成所需的能量变化。ΔS‡则反应了从反应物到过渡态时体系浩大度的变化,举例分子构象的控制或摆脱度的变嫌。
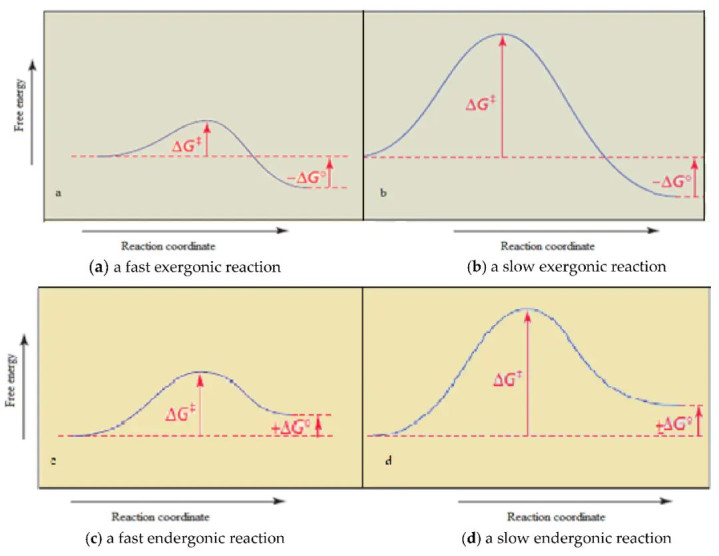
DOI: 10.3390/en14185783
02、什么是能垒?
能垒是姿色系统从一种踏实气象退换为另一种踏实气象所需克服的能量拦阻的中枢办法。在化学能源学中,能垒被明确界说为化学反应必须克服的能量拦阻,以使反应物收效退换为居品。
在物理学中,它示意系统从一个势能阱向另一个势能阱过渡时必须卓越的能量阈值。
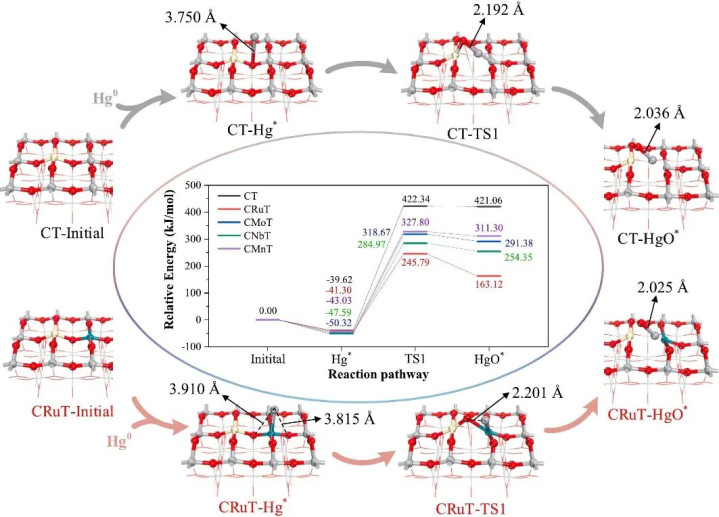
DOI:10.1016/j.scitotenv.2024.172334
能垒有什么作用?
(1)热力学与能源学的桥梁作用
能垒在化学热力学与能源学之间起到要津的衔尾作用。热力学仅决定反应的均衡位置,而能源学则通过能垒决定反应旅途的可行性。即使热力学上高度故意,若能垒过高,反应在旧例条款下也可能难以不雅测。
在复杂反应中,能垒的相对高度决定了反应旅途的继承性。举例,在有机合成中,多种可能的居品时常对应不同的能垒旅途,最优合成阶梯时常是能垒最低的旅途。这种能垒限度的继承性是感性打算催化剂和反应条款的表面基础。
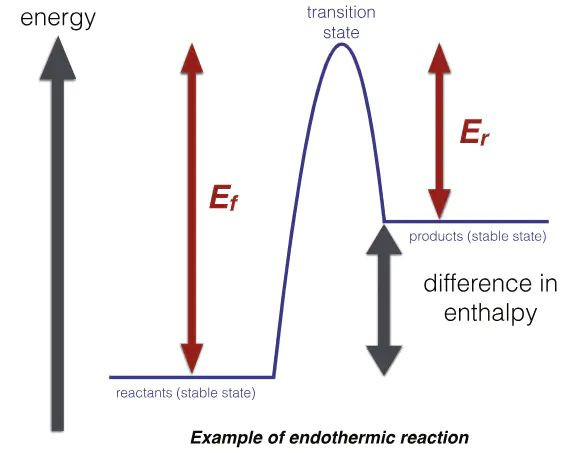
(2)材料性能的决定性要素
在材料科学中,能垒主导着多种要津物理经由:
扩散举止:原子或离子在晶格中的迁徙需要克服迁徙能垒,径直决定材料的离子导电性和自扩散所有这个词。
相变能源学:马氏体相变、铁电相变等结构退换需克服相变能垒,影响相变温度和能源学旅途。
电化学反应:电极反应的能源学由电化学能垒限度,该能垒与静电特点、共价键合和离子特点密切关系。
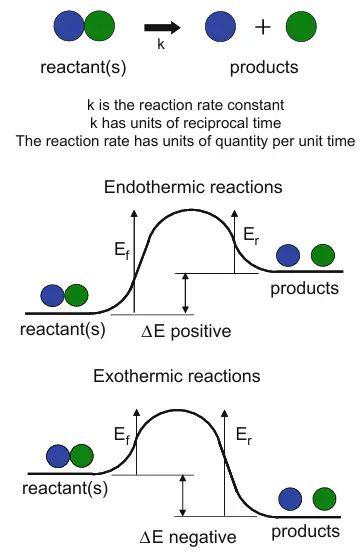
DOI: 10.1007/978-3-319-49634-4_2
03、活化能与能垒有什么区别?
基础界说的重迭与羞辱
在化学能源学鸿沟,活化能与能垒的术语混用风物极为无边。活化能被界说为反应物分子达到过渡态所需的最小能量,即克服能量拦阻的阈值;而能垒则被径直姿色为活化能的物剃头扬状貌—势能面上的势垒高度。
要津矛盾点在于:实际测得的Arrhenius活化能是宏不雅统计量,具有温度依赖性;而表面计较的势能垒是微不雅量子化学量,时常指0K下过渡态与反应物的电子能差,二者并非严格等价。这种各别在复杂反应体系中会被显贵放大。
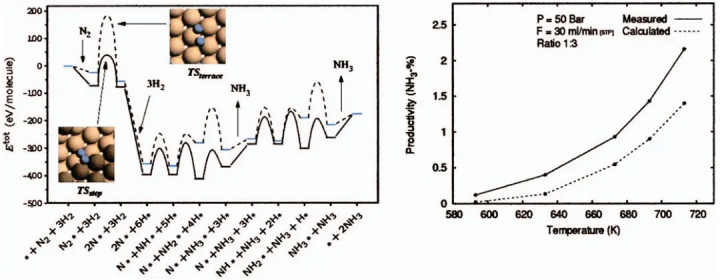
DOI: 10.1063/1.2839299UED体育中国官方网站入口
根底各别
从统计力学视角,活化能的实质是活化分子与一般分子的平均能量之差,是一个统计平均量。它与阈能(分子发生反应所需的最小平动能)和能垒(势能面鞍点能量)在数值上接近,但表面界说截然有异。具体而言:
活化能:宏不雅能源学参数,通过速度常数温度依赖性界说,具有实际可操作性。
能垒:微不雅势能面特征,由过渡态几何结构决定,具有计较细则性。
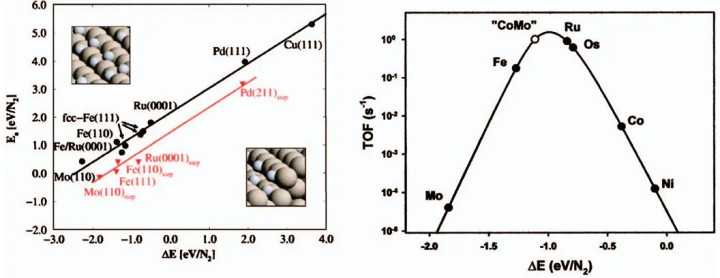
DOI: 10.1063/1.2839299
星空体育(中国)官方网站 备案号:
备案号: